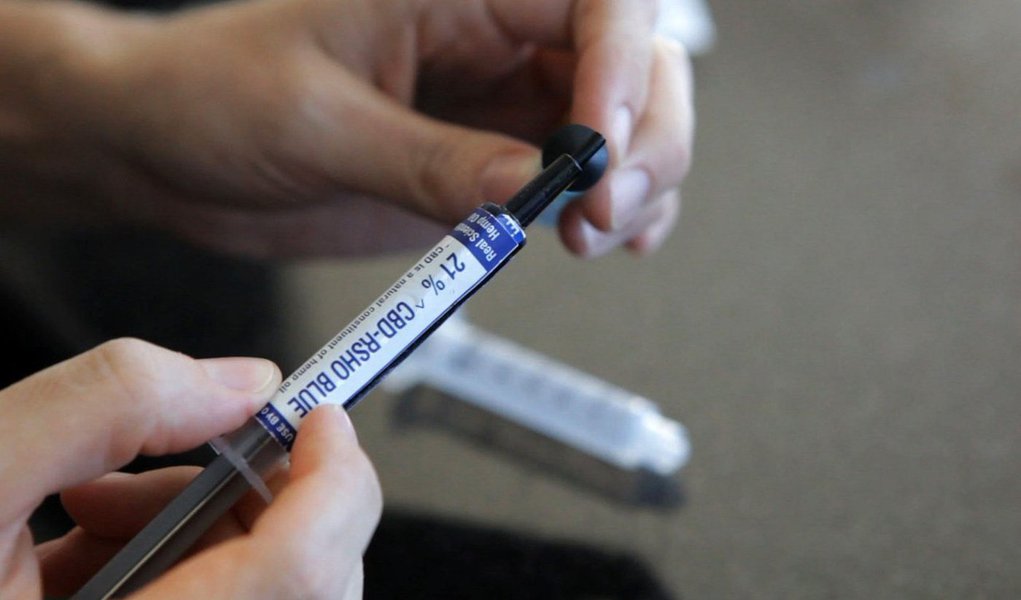
Anvisa já deu autorização a 37 pedidos de importação do canadibiol
No Brasil, a importação de medicamentos sujeitos a controle especial sem registro no país, por pessoa física, é possível por meio de pedido excepcional de importação para uso pessoal. O prazo médio das liberações, de acordo com o órgão, é de uma semana
✅ Receba as notícias do Brasil 247 e da TV 247 no canal do Brasil 247 e na comunidade 247 no WhatsApp.
Paula Laboissière, repórter da Agência Brasil - A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou, desde abril deste ano, 37 dos 59 pedidos de importação de medicamentos a base de canabidiol (CBD). Segundo a agência, os demais pedidos incluem dois oriundos de ações judiciais, nove com pendência de documentação e seis que foram protocolados recentemente e estão em análise. O prazo médio das liberações, de acordo com o órgão, é de uma semana.
A agência reforçou que, no Brasil, a importação de medicamentos sujeitos a controle especial sem registro no país, por pessoa física, é possível por meio de pedido excepcional de importação para uso pessoal. “Havendo esse pedido formal, acompanhado de prescrição médica, laudo médico e o termo de responsabilidade, a Anvisa analisará a possibilidade de autorizar a aquisição.”
Ainda de acordo com a Anvisa, o pedido de excepcionalidade é necessário porque medicamentos sem registro no país não contam com dados de eficácia e segurança registrados. Nesse caso, cabe ao profissional médico a responsabilidade pela indicação do produto, especialmente na definição da dose e das formas de uso.
Para dar início ao pedido excepcional de importação para uso pessoal, é necessário enviar uma solicitação ao gabinete do diretor-presidente da agência e apresentar os seguintes documentos originais:
- Prescrição médica contendo obrigatoriamente nome do paciente e do medicamento, posologia, quantitativo necessário, tempo de tratamento, data, assinatura e carimbo do médico (com CRM).
- Laudo médico contendo CID e nome da patologia, descrição do caso, justificativa para uso de medicamento não registrado no Brasil, em comparação com as alternativas terapêuticas já existentes registradas pela Anvisa.
- Termo de responsabilidade assinado pelo médico e paciente/responsável legal.
- Formulário de solicitação de importação excepcional de medicamentos sujeitos a controle especial preenchido e assinado pelo paciente ou responsável legal.
Para dar celeridade ao processo, a Anvisa ressaltou que uma cópia eletrônica da solicitação deverá ser encaminhada para os seguintes e-mails: gadip.assessoria@anvisa.gov.br; med.controlados@anvisa.gov.br e uniap@anvisa.gov.br.
Assine o 247, apoie por Pix, inscreva-se na TV 247, no canal Cortes 247 e assista:
Comentários
Os comentários aqui postados expressam a opinião dos seus autores, responsáveis por seu teor, e não do 247